ミッションと概要
当研究室では、BRCが各リソース、特に実験動物および幹細胞をより高度なクオリティにて維持供給するために必要な遺伝関連技術開発を行う。
また、これらの技術が広く研究コミュニティに活用されるべく、研修事業を行う。
技術開発
研究内容 2019年版
1.体細胞核移植クローン技術の開発
体細胞核移植によるクローン技術は、希少な系統の保存および新規モデル動物作出などに有用な技術であるが、未だにクローン個体の作出効率は低く、技術的改善が必要である。これまで我々は、マウスをモデルとして様々な細胞種・系統からクローン個体を作出してきた。その一方で、微小サンプルからの遺伝子発現およびエピゲノム解析技術を応用することにより、クローン胚で起こる様々なエピゲノム異常を同定してきた。
代表的な遺伝子発現・エピゲノム異常として、本来X染色体から起こる遺伝子発現がクローン胚では大規模に抑制されていること、そしてこれがXist遺伝子の異常な活性化に起因することを発見した(Inoue et al., Science, 2010)。このXistの過剰発現は、Xistの遺伝的ノックアウトもしくはsiRNAによるノックダウンで補正することができ、その結果9-10%程度までクローン個体の作出効率を上げることに成功した。(Inoue et al., Science, 2010; Matoba et al., PNAS, 2011)。
また、クローン胚の初期発生阻害因子としてヒストンH3の9番目リジンのトリメチル化(H3K9me3)を同定した(Matoba et al., Cell, 2014)。
このH3K9me3はヒストン脱メチル化酵素であるKdm4をクローン胚で発現させることで除去でき、その結果クローン個体の作出効率を8-9%程度まで大幅に改善することに成功した(Matoba et al., Cell, 2014)。
さらに最近では、Xist遺伝子の発現補正とKdm4によるH3K9me3の除去技術を組み合わせることで、マウスのクローン作出効率を最大23%にまで高めることに成功している(Matoba et al., Cell Stem Cell, 2018)。
しかしながら、このような最適化したクローン胚でもまだ受精胚と比べると個体の作出効率は半分以下と低く、さらにクローン胚特有の胎盤の形成異常が認められる。
最近我々はその原因の候補として、母性H3K27me3によるゲノムインプリンティングの喪失が関与している可能性を見出した(図1, Okae et al., Hum Mol Genet, 2014; Hirose et al., Epigenetics, 2018; Matoba et al., Cell Stem Cell, 2018)。
通常受精胚では母方由来の遺伝子の一部がH3K27me3によって抑制されており、その結果として父方発現を示すが、クローン胚ではH3K27me3による抑制が存在せず、両アレルから過剰に発現していることが明らかになった(Matoba et al., Cell Stem Cell, 2018)。
このような異常を示すインプリント遺伝子は、多くが胎盤の形成に関与している。
最近我々はそれらの遺伝子の一部であるSfmbt2 マイクロ (mi) RNAやSlc38a4が正常な胎盤形成に必須であることを示し(Inoue et al., Cell Rep., 2017; Matoba et al., PNAS, 2019)、その内Sfmbt2 miRNAの発現補正がクローン胚の胎盤形成異常を改善することを明らかにした(図2, Inoue et al., in revision)。
今後もH3K27me3によるインプリント遺伝子群のクローン胚胎盤形成に対する関与を解明することで、クローン胚の作製効率および品質(特に胎盤)を改善することが期待される。
さらに、ドナー細胞でのゲノム編集技術と組み合わせることで、クローン技術は医学生物学研究に有用な実験動物モデルの作出にさらに貢献できると考えられる。
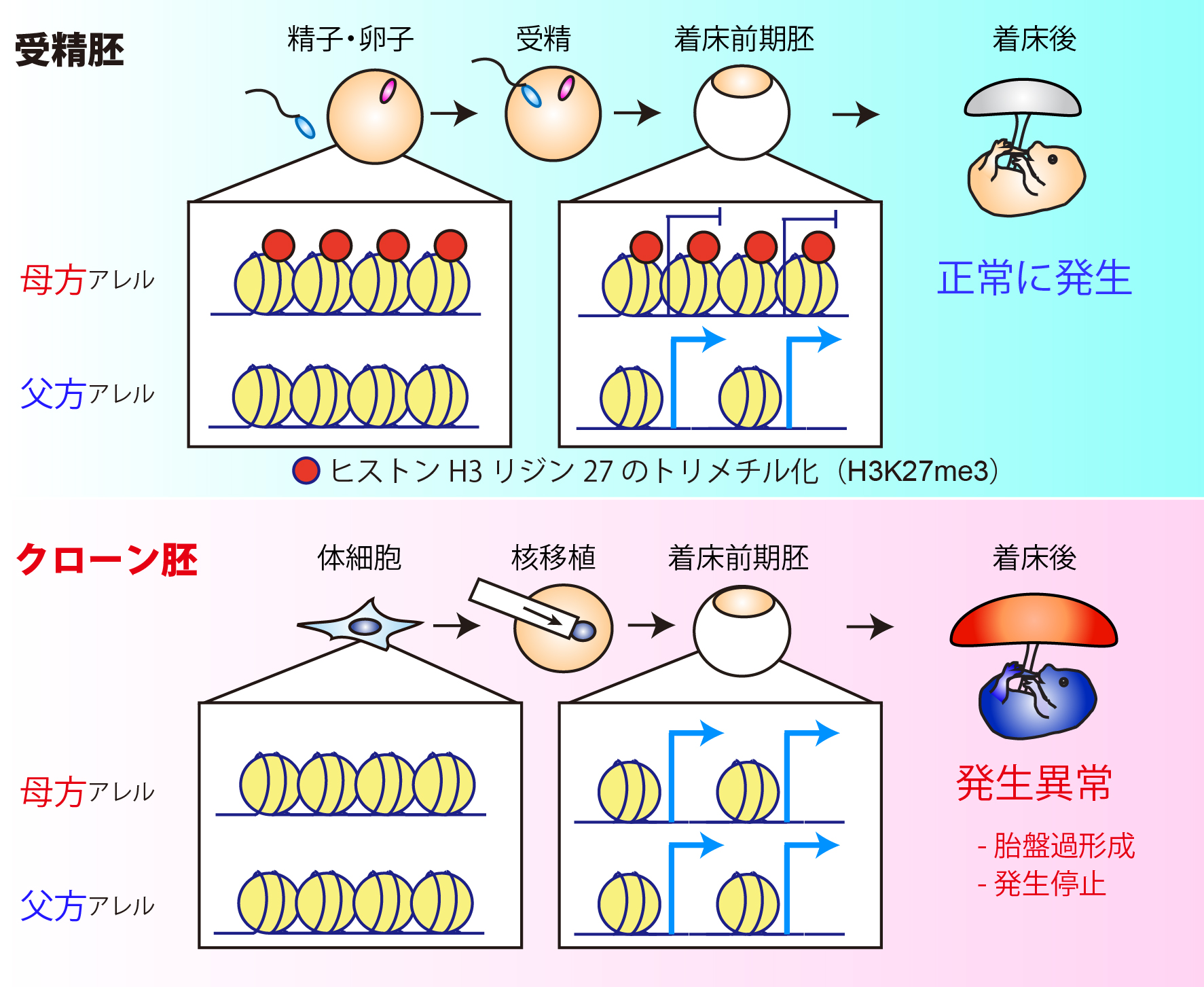
図1:クローン胚胎盤におけるH3K27me3ゲノムインプリンティングの喪失
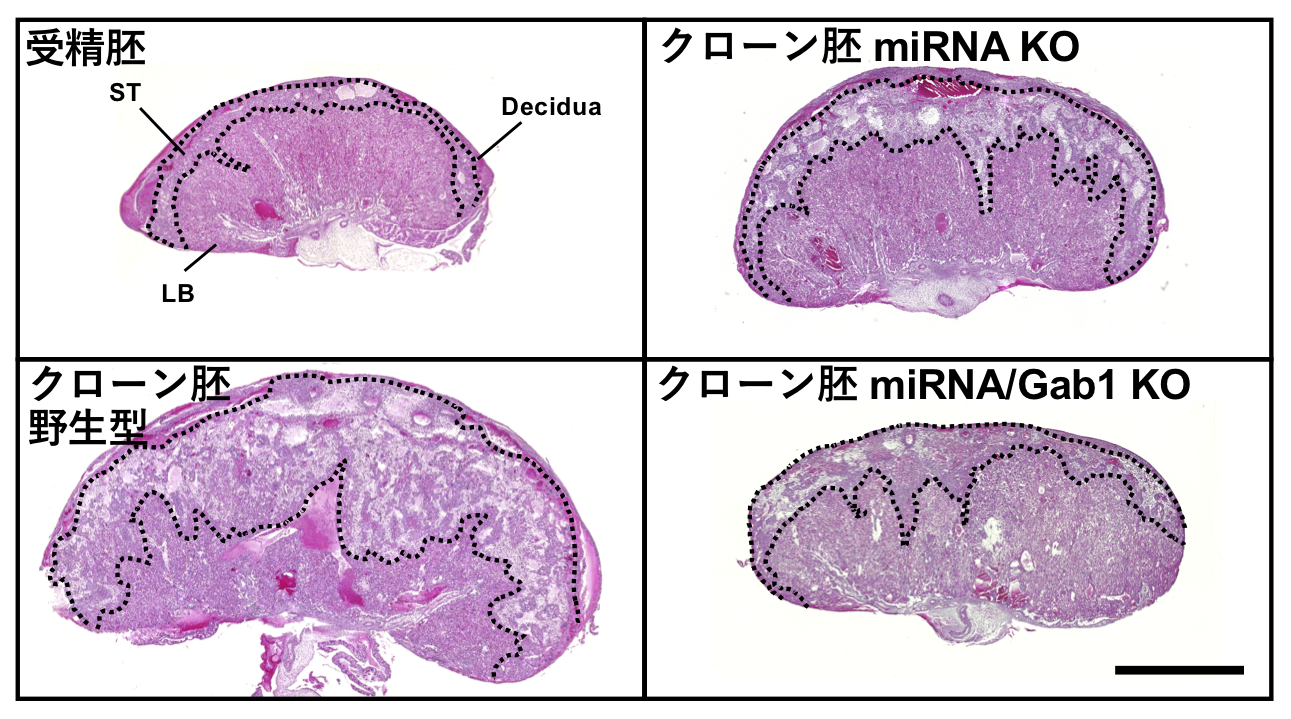
図2:受精胚、野生型クローン胚、Sfmbt2 miRNA KOクローン胚の胎盤形態
2.顕微授精技術の開発
一次精母細胞を用いた顕微授精は、すでに産仔獲得の報告がされているが、その成功率は4%以下と、初期のマウス体細胞クローン成功率に匹敵するほど低率である (Ogura et al., PNAS, 1998; Miki et al., J Reprod Dev, 2006)。
その原因として、一次精母細胞の染色体が卵子内で減数分裂を進行する際、染色体分離エラーが高頻度に生じることが挙げられている。
そこで、理化学研究所生命機能科学研究センターの京極博久ら(Dev Cell 2017)が報告した『細胞質サイズを小さくした卵子』の、紡錘体極の安定化・紡錘体チェックポイントの正確化を利用して、一次精母細胞の顕微注入卵として用いたところ、
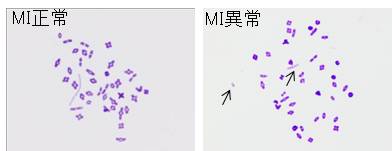
一次精母細胞由来染色体の紡錘体赤道面への整列の正確性が向上し、その後の染色体分離エラーの減少が染色体標本より確認された(下表および図)。
操作胚をレシピエントマウスに胚移植した結果、20-30%の産仔率が認められた(旭川医大日野敏昭先生との共同研究)。
表:一次精母細胞注入胚の染色体解析
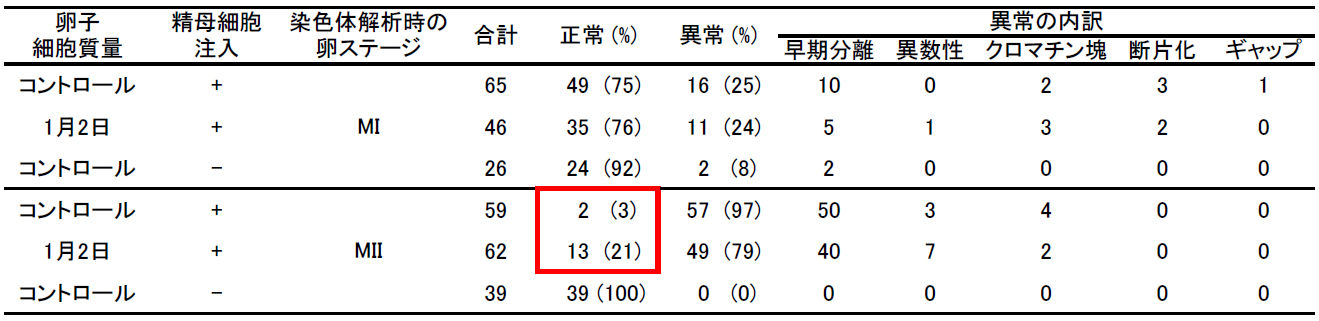
図:細胞質サイズを小さくした卵子を用いた一次精母細胞注入胚の染色体解析

3.効率的な胚・配偶子の凍結保存法の開発
胚凍結が困難な野生由来の異種マウス(M. spicilegus)であるZBN/MsとSPI/TUAの2系統から樹立したES細胞をICRの8細胞期胚および胚盤胞へ注入した結果、異種間キメラマウスの作出に成功した。現在、交配実験を進めており、ES細胞由来の産子が得られれば、ES細胞による異種マウス系統の長期保存が可能となる。

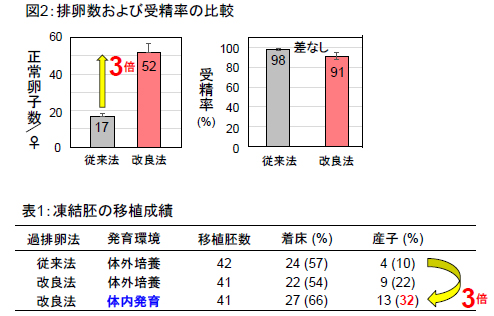
過排卵と胚発生が困難な近交系マウスの代表とされるA系統で、プロゲステロン投与による性周期同期化と抗インヒビン血清投与を組み合わせた過排卵法 (Hasegawa et al., Biol Reprod, 2016)により、正常卵子数が17個から52個に増加した。さらに体外受精後に前核期で胚移植を行い体内で2細胞期に発生した胚をガラス化保存することで胚移植後の産子数を改善でき、
雌1匹からの産子獲得効率を1.7匹から15.1匹に増加できた。
4.新規幹細胞および新規動物モデルの開発
栄養膜幹細胞 (trophoblast stem cell, TS細胞) は胚盤胞の栄養外胚葉から樹立される未分化な胎盤系列の培養幹細胞であり、胚発生の研究に有用なツールである。
当研究室は過去にTS細胞が未分化性の異なる不均一な集団から構成されていることを明らかにし(Motomura et al., Biol Reprod., 2016)、TS細胞の品質を安定化させるための技術改良が必要であることを示してきた。
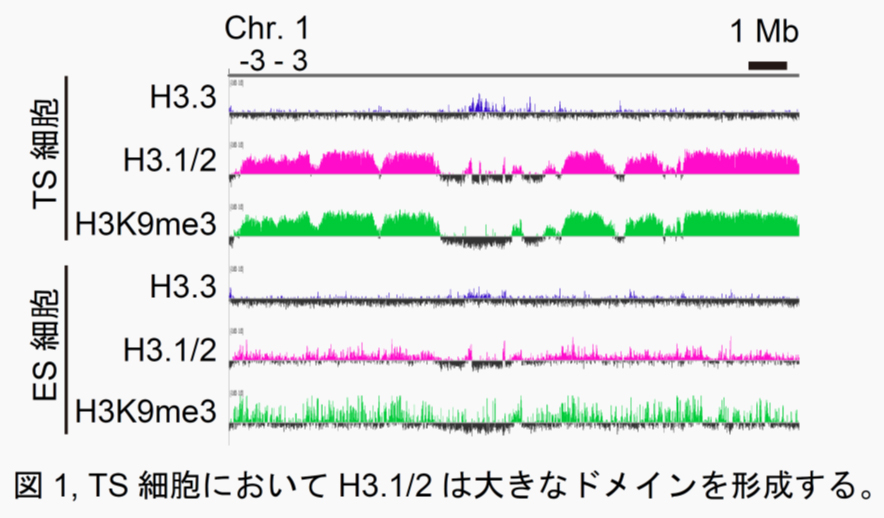
現在、ヒストンH3のバリアント、H3.1とH3.2 (=H3.1/2) がTS細胞のidentityの確立に重要である可能性が得られているため、その詳しい解析を行っている。
具体的に、H3.1/2がH3K9me3を制御することでTS細胞に特異的なクロマチン構造を形成していることが分かった (図1)。更にTS細胞において、H3.1/2をクロマチンに組み込む因子であるP150を欠損させたところ、TS細胞のマーカー遺伝子の発現量が減少し、ES細胞のマーカー遺伝子であるOct3/4の発現量が増加した。これらの結果から、H3.1/2を制御することによって、より質の高いTS細胞を維持できる可能性を考えている。
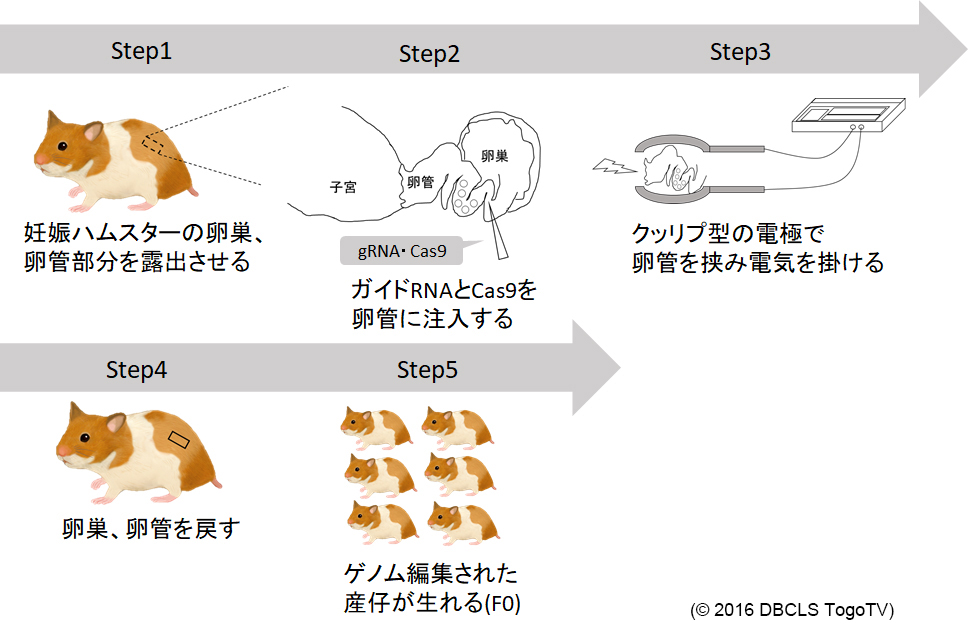
昨年度に引き続き、マウスで明らかにされていない遺伝子の機能を明らかにするために、in vivo CRISPR/Cas9(GONAD法)(図)によるノックアウトハムスター作出を行い (Hirose et al., PNAS, 2020)、 ATP 感受性カリウムチャネルサブユニットKir6.2のノックアウトに成功した。
今後、ホモノックアウト個体の糖代謝を解析する予定である。
5.技術研修
2016年度から2019年度において、所外からの研修生を対象に以下の研修を行った。
- 2016年10月 「マウス精子・胚の凍結保存方法に関する技術研修
~BRC新過排卵法と次世代マウスの早期作出法~」 - 2017年12月 「マウス顕微授精技術に関する技術研修」
- 2018年2月 「マウス顕微授精技術に関する技術研修」
- 2018年10月 「マウスの精子・胚の凍結保存方法に関する技術研修
~効率的な過排卵、若齢雄を用いた体外受精~」 - 2018年12月 「マウスの精子・胚の凍結保存方法に関する技術研修
~効率的な過排卵、若齢雄を用いた体外受精~」 - 2019年11月 「マウス顕微授精技術に関する技術研修」
- 2019年12月 「マウス顕微授精技術に関する技術研修」
